,,ტრაქტორი გადაბრუნდა და შიგ მსხდომი მამა-შვილი მოიყოლა...“ - ტრაგედია კახეთში
1751140131
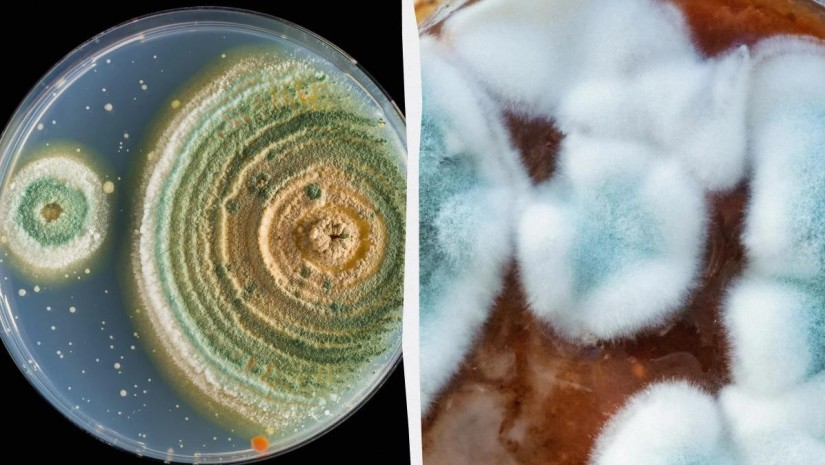
მკვლევრებმა სასიკვდილოდ საშიში სოკო — Aspergillus flavus — კიბოს საწინააღმდეგო საშუალების შესაქმნელად გამოიყენეს. ეს აღმოჩენა განსაკუთრებით მნიშვნელოვანია, რადგან აღნიშნული ტოქსიკური სოკო, რომელიც სოფლის მეურნეობის კულტურებს აზიანებს, ისტორიულად „ცუდი რეპუტაციით“ არის ცნობილი.
ის უკავშირდება იმ არქეოლოგების სიკვდილთან, რომლებიც მუშაობდნენ ძველ სამარხებში. მაგალითად, 1922 წელს ტუტანხამონის სამარხის გახსნის შემდეგ რამდენიმე მკვლევარი დაუდგენელი სიკვდილით გარდაიცვალა, რამაც საფუძველი დაუდო ცნობილი „ფარაონის წყევლას“, — წერს Interesting Engineering. მოგვიანებით გაჩნდა ჰიპოთეზა, რომ სიკვდილის მიზეზი შესაძლოა ძველ სამარხში ჩასაფრებული სოკოს ინფექცია ყოფილიყო.
მსგავსი ტრაგედია მოხდა 1970-იან წლებში პოლონეთში: მეცნიერების ჯგუფიდან ათი ადამიანი რამდენიმე კვირაში გარდაიცვალა მას შემდეგ, რაც კაზიმირ IV-ის სამარხი მოინახულეს. მიზეზად სწორედ Aspergillus flavus დასახელდა — სოკო, რომელიც ცნობილია თავისი ძლიერ ტოქსიკურობით.
რისთვის არის საშიში ასპერგილუსი ადამიანისათვის და როგორ იქცა იგი „საწამლავიდან წამლად“?
Aspergillus flavus — სოკო, რომლის ყვითელი სპორებიც, თუნდაც ათასწლეულების შემდეგ, კვლავ ინარჩუნებს სიცოცხლისუნარიანობას და საშიშია ადამიანის ჯანმრთელობისთვის. განსაკუთრებით საფრთხეს უქმნის იმ ადამიანებს, რომლებსაც დაქვეითებული აქვთ იმუნური სისტემა — მათთვის სოკოს სპორებით გამოწვეული ფილტვების მძიმე დაზიანება შესაძლოა ფატალური აღმოჩნდეს.
თუმცა სწორედ ეს „მიკრობული ბოროტმოქმედი“ გახდა მეცნიერული გარღვევის წყარო კიბოს წინააღმდეგ ბრძოლაში. პენსილვანიის უნივერსიტეტის მეცნიერებმა, პროფესორ შერი გაოს ხელმძღვანელობით, Aspergillus flavus-დან ახალი ტიპის მოლეკულების ოჯახი გამოყვეს, რომლებსაც კიბოს საწინააღმდეგო პოტენციალი გააჩნიათ.
სოკოების მედიცინაში გამოყენება სენსაციად უკვე აღარ ითვლება — კაცობრიობამ მათგან არაერთი სასარგებლო ნაერთი მიიღო. ყველაზე ცნობილი მაგალითია პენიცილინი, რომელიც 1928 წელს აღმოაჩინეს Penicillium notatum-ისგან და რომელმაც ანტიბაქტერიული თერაპიაში რევოლუცია მოახდინა.
გენეტიკური ანალიზის საშუალებით მკვლევრებმა შეძლეს სოკოს მიერ წარმოქმნილი RiPP-ნაერთების (რიბოსომულად სინთეზირებული და პოსტტრანსლაციურად მოდიფიცირებული პეპტიდები) წყაროს დადგენა და აღმოაჩინეს უნიკალური მოლეკულების კლასი, რომელიც ერთმანეთთან გადაჯაჭვული რგოლოვანი სტრუქტურით გამოირჩევა. მათ ამ ნაერთებს ასპერიგიმიცინები (asperigimycins) უწოდეს.
ასპერიგიმიცინების პოტენციალი თითქმის მაშინვე გახდა ცხადი: როდესაც ეს ნაერთები ადამიანის ლეიკემიის (სისხლის კიბო) უჯრედებზე გამოცადეს, ოთხიდან ორმა ვარიანტმა გამოხატული ანტიკიბოსური ეფექტი აჩვენა — და ეს ყოველგვარი ქიმიური მოდიფიკაციის გარეშე.
თუმცა ნამდვილი გარღვევა მოხდა მას შემდეგ, რაც მეცნიერებმა ასპერიგიმიცინის მოლეკულას მცირე მოდიფიკაცია ჩაუტარეს — მას ლიპიდური (ცხიმოვანი) მოლეკულა დაამატეს. შედეგად, ახალი ფორმულების ეფექტიანობა გაუტოლდა უკვე არსებულ, FDA-ს მიერ დამტკიცებულ პრეპარატებს — ციტარაბინსა და დაუნორუბიცინს, რომლებიც ლეიკემიის სამკურნალოდ გამოიყენება.
როგორ გაზარდა ლიპიდმა ეფექტიანობა?
მეცნიერებმა გამოავლინეს მოლეკულური მექანიზმი: აღმოჩნდა მნიშვნელოვანი გენი — SLC46A3, რომელიც მოქმედებს როგორც „კარები“, რითაც ასპერიგიმიცინებს ეძლევათ საშუალება დიდი რაოდენობით შეაღწიონ ლეიკემიის უჯრედებში.
შემდგომმა კვლევებმა ცხადყო, რომ ეს ნაერთები უშუალოდ აფერხებენ უჯრედის დაყოფის პროცესს — ისინი ბლოკავენ მიკროტუბულების წარმოქმნას, რაც აუცილებელია უჯრედის დაყოფისთვის.
„რაკის უჯრედები უკონტროლოდ იყოფიან. ეს ნაერთები სწორედ ამ პროცესს ანადგურებენ,“ — განმარტა პროფესორმა შერი გაომ.